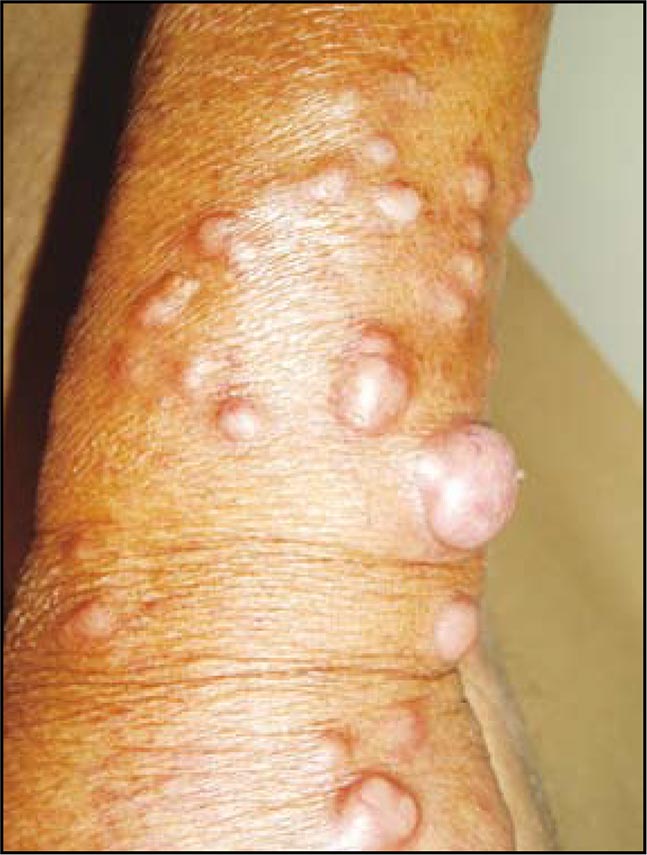
Lepra
Palabras clave:
Micobacterium leprae, lepra, pielResumen
La lepra es una enfermedad granulomatosa crónica de carácter sistémico causada por el Mycobacterium leprae (bacilo de Hansen). Se transmite de persona a persona y tiene un período largo de incubación (entre dos y seis años). Existen dos formas clínicas polares: lepra lepromatosa (multibacilar) y lepra tuberculoide (paucibacilar), con otras formas intermedias de características híbridas. El diagnóstico se basa en la sospecha clínica y se completa con el examen bacteriológico e histopatológico. La prueba de Mistusa (intradermorreacción que suele ser negativa en la forma lepromatosa y positiva en la tuberculoide) es útil para determinar el estado inmunológico del paciente. Los fármacos más utilizados para tratar esta
enfermedad son la dapsona, la rifampicina y la clofazimina. El diagnóstico temprano, la terapia apropiada y el manejo multidisciplinario mejoran el pronóstico y la calidad de vida de los pacientes con esta enfermedad.
Biografía del autor/a
Ana María Rivas
RI Dermatología. Universidad Pontificia Bolivariana. Medellín, Colombia.
Luz Marina Gómez
Dermatóloga. Profesora titular, Universidad Pontificia Bolivariana. Medellín, Colombia.
Referencias bibliográficas
2. Guías de promoción de la salud y prevención de enfermedades en la salud pública. Tomo III. Guía 18. Guía de atención de la lepra. 2007. p 29 URL disponible en: http://www.minproteccionsocial.gov.co/VBeContent/library/documents/DocNewsNo16159DocumentNo4194.PDF. Ingreso 4 noviembre de 2007.
3. Rodríguez G, Orozco LC. Lepra. Santafé de Bogotá: Instituto Nacional de Salud. 1996.
4. De Zubiria R, Rodríguez G. Historia de la lepra, ayer, hoy y mañana. URL disponible en: http://anm.encolombia.com/academ25161-lepra.htm ingreso 5 de noviembre de 2007.
5. Historia sanatorio Agua de Dios. URL disponible en: http://www.sanatorioaguadedios.gov.co/quienes/quienes_historia.htm Ingreso 5 de noviembre de 2007.
6. World Health Organization. Leprosy Global Situation. URL disponible en: http://www.who.int/lep/situation/en/ Ingreso 5 de noviembre de 2007.
7. Organización Panamericana de la Salud. Situación de la lepra en la Región de las Américas. URL disponible en: http://www.paho.org/Spanish/AD/DPC/CD/lep-americas.htm Ingreso 5 de noviembre de 2007.
8. Sasaki S, Takeshita F, Okuda K, Ishii N. Mycobacterium leprae and leprosy: a compendium. Microbiol Immunol. 2001;45:729-36.
9. Cho SN, Cellona RV, Villahermosa LG, Fajardo TT Jr, Balagon MV, Abalos RM, et al. Detection of phenolic glycolipid I of Mycobacterium leprae in sera from leprosy patients before and after start of multidrug therapy. Clin Diagn Lab Immunol. 2001;8:138–42.
10. Walker SL, Lockwood DN. The clinical and immunological features of leprosy. Br Med Bull. 2006;77-8:103-21.
11. De Souza FC, Marcos EV, Ura S, Opromolla PA, Nogueira ME. Comparative study between the Mitsuda test and the human leukocyte antigens in leprosy patients. Rev Soc Bras Med Trop. 2007;40:188-91.
12. Gamboa LA, Paredes M. Compromiso neurológico en la lepra. Univ med. 2003; 44 :217-223
13. Gómez JR, Moll F. Lepra: enfermedad olvidada. Situación actual y trabajo sobre el terreno. Enf Emerg. 2005;7:110-9.
14. Spiering E, De Boer T, Zulianello L, Ottenhoff TH. Novel mechanisms in the inmunopatogenesis of leprosy nerve damage: The role of Schwann cells, T cells and Mycobacterium leprae. Immunol. Cell Biol. 2000; 78: 349-55.
15. Walker SL, Lockwood DN. Leprosy. Clin Dermatol. 2007 M; 25:165-72.
16. Araújo MG. Leprosy in Brazil. Rev Soc Bras Med Trop. 2003; 36:373-8.
17. Chimenos E, Pascual M, Pinol C, Vinals H, Rodríguez de Rivera ME, López J. Lepromatous leprosy: a review and case report. Med Oral Patol Oral Cir Bucal. 2006;11: E474-9.
18. Ffytche TJ. The prevalence of disabling ocular complications of leprosy: a global study. Indian J Lepr 1998;70:49 – 9.
19. Lewallen S, Courtright P. A overview of ocular leprosy after 2 decades of multidrug therapy. Int Ophthalmol Clin. 2007;47:87-101.
20. Burstein Alva Z. La lepra (Enfermedad de Hansen). Parte II: reacciones lepróticas y secuelas. Rev Peru Med Exp Salud Publica. 2005; 22: 151-3.
21. Van Brakel WH, Khawas IB, Lucas SB. Reactions in leprosy: an epidemiological study of 386 patients in West Nepal. Lepr Rev 1994; 65:190–203.
22. Reyes Flórez O. La reacción leprosa una revisión. Derm. Venez. 2000. 38 : 85-95.
23. Fernández JL, Rangel Mayoral JF, Liso Rubio FJ. Revisión de la enfermedad de Hansen. Farm Hosp. 2004; 28: 123-9.
24. Boggild AK, Keystone JS, Kain KC. Leprosy: a primer for Canadian physicians. CMAJ. 2004 Jan 6;170:71-8.
25. Croft RP, Richardus JH, Smith WCS. Field treatment of acute nerve function impairment in leprosy using a standardized corticosteroid regimen — first year’s experience with 100 patients. Lepr Rev 1997;68:316-25.
26. Pocaterra L, Jain S, Reddy R, Muzaffarullah S, Torres O, Suneetha S, et al. Clinical course of erythema nodosum leprosum: an 11-year cohort study in Hyderabad, India. Am J Trop Med Hyg 2006;74:868–79.
27. Sarno EN, Grau GE, Vieira LM, Nery JA. Serum levels of tumour necrosis factor-alpha and interleukin-1 beta during leprosy reactional states. Clin Exp Immunol 1991;84:103- 8.
28. Sampaio EP, Duppre NC, Nery JA, Moreira AL, Sarno EN. Development of giant reaction in response to PPD skin test in lepromatous leprosy patients. Int J Lepr Other Mycobact Dis. 1993;61:205-13.
29. Manandhar R, LeMaster JW, Roche PW. Risk factors for erythema nodosum leprosum. Int J Lepr Other Mycobact Dis. 1999;67:270 -8.
30. Rijal A, Agrawal S, Agarwalla A, Lakhey M. Bullous erythema nodosum leprosum: a case report from Nepal. Lepr Rev 2004;75:177- 80.
31. Como reconocer y tratar las reacciones leprosas. Guía de aprendizaje No. 2. ILEP. URL disponible en: http://www.ilep.org.uk/documents/lg2sp.pdf Ingreso 8 de enero de 2008.
32. Helmer KA, Fleischfresser I, Kucharski-Esmanhoto LD, Neto JF, Santamaría JR. The Lucio's phenomenon (necrotizing erythema) in pregnancy. An Bras Dermatol. 2004; 79:205-10.
33. Costa IM, Kawano LB, Pereira CP, Nogueira LS. Lucio's phenomenon: a case report and review of the literature. Int J Dermatol. 2005 ;44:566-71.
34. Sehgal VN. Lucio's phenomenon/erythema necroticans. Int J Dermatol. 2005;44:602-5.
35. Rodríguez G, Pinto R, Laverde C, Sarmiento M, Riveros A, Valderrama J, et al. Recidivas postratamiento de la lepra multibacilar. Biomédica. 2004;24: 133-9.
36. WHO Expert Committee on Leprosy. 7th report. no. 874 of Technical Report series. Geneva: World Health Organization; 1998.
37. URL disponible en www.clinicalevidence.com. Fecha de ingreso 15 de Enero de 2008.
38. Girdhar BK, Girdhar A, Kumar A. Relapses in multibacillary leprosy patients: effect of length of therapy. Lepr Rev 2000;71:144–53.
39. Efficacy of single dose multidrug therapy for the treatment of single-lesion paucibacillary leprosy. Single-lesion Multicentre Trial Group. Indian J Lepr 1997;69:121-9.
40. Zodpey SP. Protective effect of bacillus Calmette Guerin (BCG) vaccine in the prevention of leprosy: a meta-analysis. Indian J Dermatol Venereol Leprol. 2007;73:86-93.
Cómo citar
Descargas
Descargas
Publicado
Cómo citar
Número
Sección
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |