Reproducibilidad del método de coloración Naranja de Acridina Fenólica para basiloscopia de lepra y concordancia con el Ziehl Neelsen
Palabras clave:
Mycobacterium leprae, NAF, ZNResumen
Aunque el diagnóstico de lepra es clínico,se hace necesario contar con pruebas complementarias como la baciloscopia, que ayuden a su clasificación, control del tratamiento y vigilancia. Puesto que el método de tinción tradicional Ziehl Neelsen (ZN) presenta como desventaja un prolongado tiempo de lectura en muestras con una carga bacilar baja, se requiere buscar nuevas alternativas. Con tal objetivo, se evaluó la reproducibilidad (concordancia intra e interobservador) del método de coloración fluorescente Naranja de Acridina Fenólica (NAF), reportado en la literatura para el diagnóstico de la tuberculosis, y se analizó su concordancia con la coloración ZN.
El trabajo se inició con la estandarización de la colora ción y su posterior aplicación en los duplicados de 103 muestras de moco y linfa, con diferentes grados de positi vidad, provenientes de pacientes con Lepra Lepromatosa, que consultaron al Centro Dermatológico "Federico Lleras Acosta" y se realizó lectura ciega a las placas teñidas con NAF y ZN.
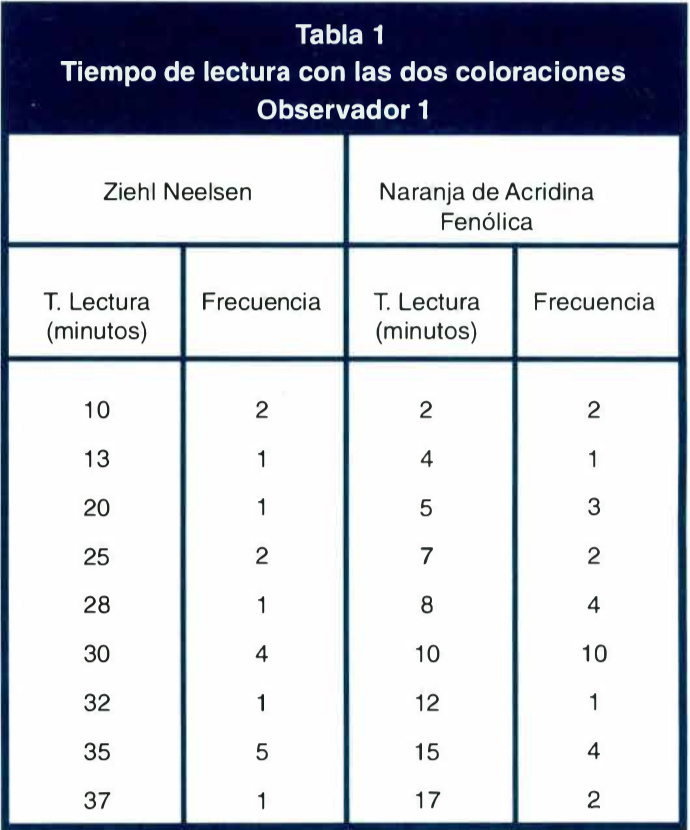
La comparación del tiempo de lectura promedio de los dos métodos de coloración fue realizada con el test de t de Student, encontrándose que este tiempo fue significati vamente menor con NAF (promedio 9.5 minutos), respec to a ZN (promedio 27.5 minutos) (t=8.2; p=0.009).
La reproducibilidad interobservador demostró ser ex celente para las muestras de moco nasal y linfa (Kappa= 1.0 y 0.91 respectivamente); la reproducibilidad intraobser vador, evaluada en muestras de linfa, demostró resulta dos buenos para ambos observadores (Kappa = 0.74 y 0.80 respectivamente). La concordancia en la lectura en tre los métodos ZN y NAF demostró ser excelente para identificar presencia o ausencia de bacilos en las mues tras de moco nasal (Kappa= 1.O) y buena para las mues tras de linfa (Kappa= 0.68). Referente al análisis del costo directo, se estableció que NAF es más económico.
Debido a la facilidad en su procesamiento, menor tiem po de lectura, reproducibilidad y economía, se recomien da utilizar este método de coloración, como alternativa al ZN, para la clasificación y seguimiento de pacientes multi bacilares.
Biografía del autor/a
María Juliana Araújo, Centro Dermatológico "Federico Lleras Acosta"
Bacterióloga, Master en Microbiología, Docente, Centro Dermatológico "Federico Lleras Acosta".
Marisol Villalobos, Pontificia Universidad Javeriana
Estudiante de Bacteriología, Pontificia Universidad Javeriana, Santafé de Bogotá.
Maritza Rey Pinzón, Centro Dermatológico "Federico Lleras Acosta"
Médica Epidemióloga, Jefe Docencia e Investigación, Centro Dermatológico "Federico Lleras Acosta", Santafé de Bogotá.
Referencias bibliográficas
2. Rodríguez G, Orozco LC. Lepra. Instituto Nacional de Salud. Bogotá, 1996, 222 p.
3. Bhutani LK. Leprosy. The Lancet 1995; 335:697-703.
https://doi.org/10.1016/S0140-6736(95)90871-4
4. Convit J, Pinardi ME. A simple method for the differentiation of Mycobacterium Leprae from other mycobacteria through routine staining technics. lnt J Leprosy 1972; 40:130-132.
5. Naranjo De P, Rodríguez G, Rodríguez J et al. La coloración de Ziehl Neelsen en histopatología biomédica 1988; 8:84-93.
https://doi.org/10.7705/biomedica.v8i3-4.1964
6. Pfaller M. Application of new technology to the detection, identification, and antimicrobial susceptibility testing of mycobacteria. Clin Microbio! lnfect Dis 1994; 329-337.
https://doi.org/10.1093/ajcp/101.3.329
7. Patterson VK, McDonald C, Miller B et al. Use of UV paralens adapter for detection of acid-fast organisms. J Clin Microbio! 1995; 33:239-241.
8. Maldonado J (ed). El laboratorio clínico y las técnicas de Biología molecular - Un matrimonio indisoluble. lladiba. 1999; 13:71-72.
9. Allen JA. Modified Ziehl-Neelsen stain for Mycobacteria. Med Lab Sci 1992; 49:99-102.
1O. Lipsky B, Gates J, Tenover F et al. Factors affecting the clinical value of microscopy for acid-fast bacilli. Rev lnfect Dis 1984; 6:214-222.
https://doi.org/10.1093/clinids/6.2.214
11. Cserni G. Auramine fluorescence for acid-fast bacilli in formalin-fixed paraffin-embedded tissues. Am J Clin Pathol 1994; 101:114.
https://doi.org/10.1093/ajcp/103.1.114
12. Drevets D, Elliott A. Fluorescence labeling of bacte riaforstudiesofintracellularpathogenesis.J lnmunol Meth 1995; 185:69-79.
https://doi.org/10.1016/0022-1759(95)00168-A
13. Kepner R, Pratt J. Use of fluorochromes for direct enumeration of total bacteria in environmental samples: past and present. Microbio! Rev 1994; 58:603- 615.
14. McCarter Y, Robinson A. Detection of acid-fast bacilli in concentrated primary specimen smears stained with rhodamine-auramine at room temperature and at 37C. J Clin Microbio! 1994; 32:2487-2489.
15. Strumpf Y, Tsang A, Schork A et al. T he reliability of gastric smears by Auramine-Rhodamine staining technique for the diagnosis of tuberculosis. Am Rev Respirat Dis 1976; 114:971-976.
16. Daniel T. The rapid diagnosis of tuberculosis: A Selective Review. J Lab Clinic Medie 1990; 116:277-282.
17. Smithwick R, Rigbie M, Ferguson R, et al. Phenolic Acridine Orange Fluorescent stain for mycobacteria. J Clin Microbio! 1995; 33:2763-2764.
18. Sackett D, Haynes R, Guyatt G et al. Clinical Epidemiology, 2a. ed. Boston/Toronto/London; Little Brown and Company (eds), 1991; 34-61.
Cómo citar
Descargas
Descargas
Publicado
Cómo citar
Número
Sección
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |