¿Onicomicosis con reacción negativa a la tinción con ácido periódico de Schiff?
Palabras clave:
Onicomicosis/patología; Onicomicosis/diagnóstico; Onicomicosis/microbiología; Micología/métodos; Histocitoquímica/métodos; Reacción del Ácido Periódico de Schiff; Metenamina/Uso DiagnósticoResumen
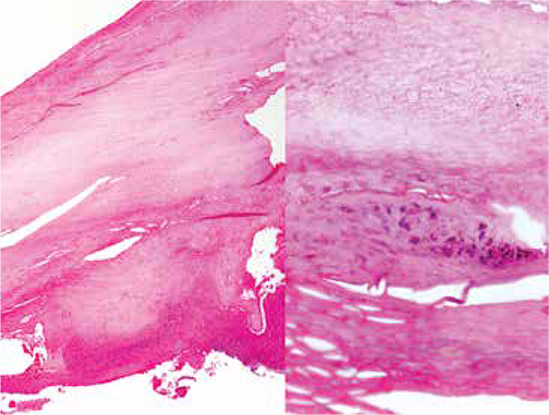
Presentamos el caso de un hombre de 43 años con una mácula marrón oscuro de varios meses de evolución en la uña del dedo gordo del pie derecho. En el estudio histopatológico de la lámina ungular, la coloración inicial de PAS fue negativa para hongos y la tinción de Grocott demostró abundantes hifas; en una segunda coloración de PAS realizada a un nivel más profundo del tejido, las hifas fueron visibles.
La biopsia de la porción distal de la lámina ungular teñida con PAS tiene una sensibilidad del 85 - 98% para el diagnóstico de onicomicosis. Cuando el PAS es negativo en una muestra con sospecha clínica de onicomicosis, la repetición de esta coloración en cortes seriados o más profundos, demuestra la presencia del hongo. La eficiencia de las tinciones de PAS y Grocott es similar y su sensibilidad aumenta con los cortes seriados, pero la coloración de Grocott es más costosa.
Biografía del autor/a
Iván Mojica
Patólogo Anatómico y Clínico, Departamento de Patología y Laboratorios, Fundación Santa Fe de Bogotá, Bogotá D.C. Instructor Asociado, Facultad de Enfermería, Universidad El Bosque, Bogotá D.C.
Viviana Arias
Profesora Asistente de Patología, Facultad de Medicina, Universidad Nacional, Bogotá D.C
Gerzaín Rodríguez
Profesor titular y Maestro universitario (jubilado), Facultad de Medicina, Universidad Nacional, Bogotá. Catedrático, Facultad de Medicina, Universidad de La Sabana, Chía, Cundinamarca.
Referencias bibliográficas
2. Berker D. Fungal Nail Disease. N Engl J Med. 2009; 360: 2108-16.
3. Mitchell T. Medical Mycology, In: Jawetz, Melnick, & Adelberg’s Medical Microbiology. 24th Ed. New York: The Mc Graw Hill companies Inc., 2007: 621-57
4. Ghannoum MA, Hajjeh RA, Scher R, Konnikov N, Gupta AK, Summerbell R, et al. A large-scale North American study of fungal isolates from nails: The frequency of onychomycosis, fungal distribution, and antifungal susceptibility patterns. J Am Acad Dermatol. 2000; 43: 641-8.
5. Faergemann J, Baran R. Epidemiology, clinical presentation and diagnosis of onychomycosis. Br J Dermatol. 2003; 149 (Supl. 65): S1–S4.
6. Chowdhary A, Randhawa HS, Sharma S, Brandt ME, Kumar S. Malassezia furfur in a case of onychomycosis: colonizer or etiologic agent. Med Mycol. 2005; 43: 87-90.
7. Zuluaga DA, de Bedout C, Tabares A, Cano LE, Restrepo A, Arango M, et al. Comportamiento de los agentes etiológicos de las onicomicosis en un laboratorio de micología de referencia (Medellín 1994 - 2003). Med Cutan Iber Lat Am. 2005; 33: 251-56.
8. Lawry MA, Haneke E, Strobeck K, Martin S, Zimmer B, Romano PS. Methods for Diagnosing Onychomycosis. A Comparative Study and Review of the Literature. Arch Dermatol. 2000; 136: 1112-16.
9. Ellis DH. Diagnosis of Onychomycosis made simple. J Am Acad Dermatol. 1999; 40(Supl. 6): S3-S8.
10. Weinberg J, Koestenblatt E. Comparison of diagnostic methods in the evaluation of onychomycosis. J Am Acad Dermatol. 2003; 49: 193-97.
11. Mondragon G. Histotechnologist to histopathologist: a method for processing specimens of nails. Dermatopathology: Practical & Conceptual. 1996 Jun [cited 2012 Oct 15]; 2(1): [about 2p.]. Available from: http://www.derm101.com/indexDPC
12. Baral J, Fusco F, Kahn H, Ramsinghani R, Phelps R. The use of nail clippings for detecting fungi in nail plates. Dermatopathology: Practical & Conceptual. 1996 Oct [cited 2012 Oct 15]; 2(4): [about 7p]. Available from: http://www.derm101.com/indexDPC
13. Reisberger EM, Abbels C, Landthaler M, Szeimies R-M. Histopathological diagnosis of onychomycosis by periodic acid Schiffstained nail clippings. Br J Dermatol. 2003; 148: 749-54.
14. Gómez LM, Massaro M, Tabares AM, Zuluaga A, Vélez JD, Vélez A y cols. Utilidad de la muestra de la lámina ungular en el diagnóstico de onicomicosis. Rev Asoc Colomb Dermatol. 2011; 19: 194-200.
15. Grocott RG. A stain for fungi in tissue sections and smears using Gomori´s methenamine-silver nitrate technic. Am J Clin Pathol. 1955; 25: 975.
16. D’Hue Z, Perkins SM, Billings SD. GMS is superior to PAS for diagnosis of onychomycosis. J Cutan Pathol. 2008; 35: 745–7.
17. Reza Kermanshahi T, Rhatigan R. Comparison between PAS and GMS stains for the diagnosis of onychomycosis. J Cutan Pathol. 2010; 37: 1041- 44.
18. Barak O, Asarch A, Horn T. PAS is optimal for diagnosing onychomycosis. J Cutan Pathol. 2010: 37: 1038 – 40.
19. Lilly KK, Koshnick RL, Grill JP, Khalil ZM, Nelson DB, Warshaw EM. Cost-effectiveness of diagnostic tests for toenail onychomycosis: A repeated-measure, single-blinded, cross-sectional evaluation of 7 diagnostic tests. J Am Acad Dermatol. 2006; 55: 620-6.
20. Weedon D. Diagnostic clues, In: Weedon D, Editor. Skin pathology. Third edition. Churchill Livingstone Elsevier, 2010: 31.
21. Wisselink G, van Zanten E, Kooistra-Smid A. Trapped in keratin; a comparison of dermatophyte detection in nail, skin and hair samples directly from clinical samples using culture and realtime PCR. J Microbiol Methods. 2011; 85: 62-6
Cómo citar
Descargas
Descargas
Publicado
Cómo citar
Número
Sección
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |