Biopsia de mucosa nasal: descripción de técnicas y comparación de los resultados con gubia versus otros instrumentos en un hospital de referencia
DOI:
https://doi.org/10.29176/2590843X.1550Palabras clave:
Biopsia, Mucosa nasal, Procedimientos diagnósticos, TécnicasResumen
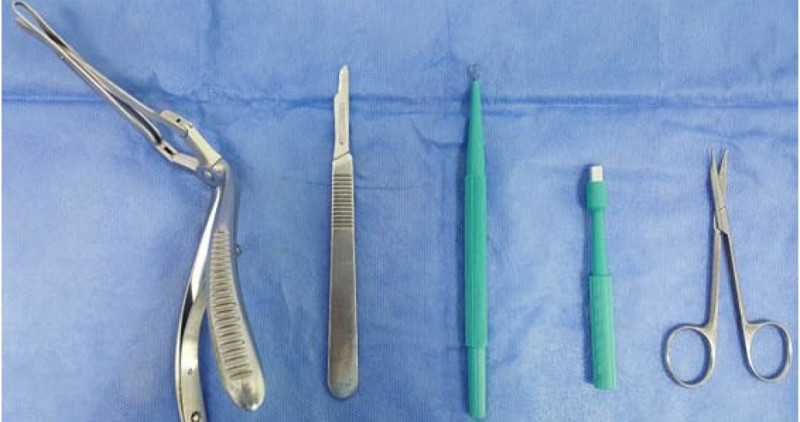
Objetivos: para la biopsia de mucosa nasal se usan diversos instrumentos, que pueden variar el resultado histológico. El propósito del estudio es describir y determinar la frecuencia de resultados histológicos satisfactorios de la biopsia tomada con gubia versus otros instrumentales en pacientes con lesiones de mucosa nasal.
Materiales y métodos: estudio de corte transversal, que incluyó registros clínicos de pacientes en quienes se realizó biopsia de mucosa nasal entre 2005 y 2016 en un hospital dermatológico en Bogotá, Colombia. Se excluyeron biopsias extrainstitucionales. Se analizaron características demográficas, clínicas y paraclínicas. El resultado satisfactorio se definió como la obtención de muestra suficiente sin presencia de artificios que impidiera al patólogo confirmar el diagnóstico. Adicionalmente, se reportó diámetro y profundidad de las muestras.
Resultados: se incluyeron 98 registros. En el 70,4% de los casos se tomó biopsia con gubia. El diámetro de la muestra con gubia fue ligeramente mayor (3., mm vs. 2,8 mm [p=0,16]). La frecuencia de resultado satisfactorio fue similar en quienes se utilizó gubia (94,2%) u otro instrumental (93,1%). No obstante, las biopsias con resultado satisfactorio fueron de mayor diámetro y profundidad.
Discusión y conclusiones: no se observaron diferencias en la frecuencia de resultados satisfactorios de acuerdo con el tipo de instrumental; probablemente la calidad de la muestra es dependiente del operador. Para aumentar la probabilidad de un resultado satisfactorio se sugiere tener una muestra con diámetro mayor de 3 mm y mínimo 2 mm de profundidad.
Biografía del autor/a
Diana Patricia Crizón-Díaz
Posgrado de Dermatología, Fundación Universitaria Sanitas, Bogotá, Colombia. Hospital Universitario Centro Dermatológico Federico Lleras Acosta, Bogotá, Colombia
Victoria Eugenia Franco
Posgrado de Dermatología, Fundación Universitaria Sanitas, Bogotá, Colombia. Hospital Universitario Centro Dermatológico Federico Lleras Acosta, Bogotá, Colombia
Claudia Carolina Colmenares
Unidad de investigación, Fundación Universitaria Sanitas, Bogotá, Colombia.
Referencias bibliográficas
2. Gul HC, Tosun F, Karakas A, Koru O, Onguru O, Mert G, et al. A case of mucosal leishmaniasis: Mimicking intranasal tumor with perforation of septum. J Microbiol Immunol Infect. 2016;49(4):604-7. doi: 10.1016/j.jmii.2013.11.007
3. Prior AJ, Calderon MA, Lavelle RJ, Davies RJ. Nasal biopsy: indications, techniques and complications. Respir Med. 1995;89(3):161-9. doi: 10.1016/0954-6111(95)90242-2
4. Rodriguez G, Pinto R. La lepra. Imágenes y conceptos. Medellín: Editorial Universidad de Antioquia; 2007.
5. Truman R, Krahenbuhl J. Viable M. leprae as a research reagent. Int J Lepr Other Mycobact Dis. 2001;69(1):1-12.
6. Milanes R, Caro C, Vélez C, Marrugo O. Diagnóstico diferencial de la rinosporidiosis: a propósito de un caso. Iatreia. 2012;25(3):272-6.
7. Jaimes A, Muvdi S, Alvarado Z, Rodríguez G. Perforation of the nasal septum as the first sign of histoplasmosis associated with AIDS and review of published literature. Mycopathologia. 2013;176(1-2):145-50. doi: 10.1007/s11046-013-9662-z
8. Reyes HD, Marquez RE, Fuste JC, Ramos VJ. Granuloma letal de la línea media como diagnóstico diferencial de la vasculitis de Wegener. Presentación de una paciente. Acta Med Centro. 2015;9(2):34-40.
9. Mallya V, Singh A, Pahwa M. Lethal midline granuloma. Indian Dermatol Online J. 2013;4(1):37-9. doi: 10.4103/2229-5178.105469
10. Fuller J. Selección del instrumental quirúrgico. En: Fuller J, Ness E (editores). Instrumentación quirúrgica: teoría, técnicas y procedimientos. 4.ª edición. México: Editorial Médica Panamericana; 2007. p. 457-9.
11. Zuber TJ. Fusiform excision. Am Fam Physician. 2003;67(7):1539-44, 1547–8, 1550.
12. Goldberg LH, Alam M. Elliptical excisions: variations and the eccentric parallelogram. Arch Dermatol. 2004;140(2):176-80. doi: 10.1001/archderm.140.2.176
13. Pickett H. Shave and punch biopsy for skin lesions. Am Fam Physician. 2011;84(9):995-1002.
14. Goldman G. The current status of curettage and electrodesiccation. Dermatol Clin. 2002;20(3):569-78, ix. doi: 10.1016/s0733-8635(02)00022-0
15. StataCorp. 2013. Stata Statistical Software: Release 13. College Station, TX: StataCorp LP.
16. Segal N, Osyntsov L, Olchowski J, Kordeluk S, Plakht Y. Nose biopsy: a comparison between two sampling techniques. Eur Arch Otorhinolaryngol. 2016;273(6):1445-8. doi: 10.1007/s00405-015-3754-y
Cómo citar
Descargas
Descargas
Publicado
Cómo citar
Número
Sección

| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |