Profilaxis con tetraciclinas para la prevención del exantema pápulo-pustular en pacientes oncológicos que van a recibir inhibidores del receptor del factor de crecimiento epidérmico
Palabras clave:
inhibidores del receptor de factor de crecimiento epidérmico (EGF), receptor del factor de crecimiento epidérmico (receptor del EGF), tetraciclinas, prevención, exantema pápulo-pustular, ensayos clínicos.Resumen
Introducción. El objetivo de esta revisión fue determinar si la profilaxis con tetraciclinas reduce la incidencia de exantema pápulo-pustular en pacientes oncológicos en manejo con inhibidores del receptor del factor de crecimiento epidérmico.
Materiales y métodos. Se hizo una revisión sistemática de la literatura científica, a partir de ensayos clínicos controlados de asignación aleatoria sobre la profilaxis con tetraciclinas en pacientes con cualquier tipo de cáncer en protocolo para uso de inhibidores del receptor del factor de crecimiento epidérmico.
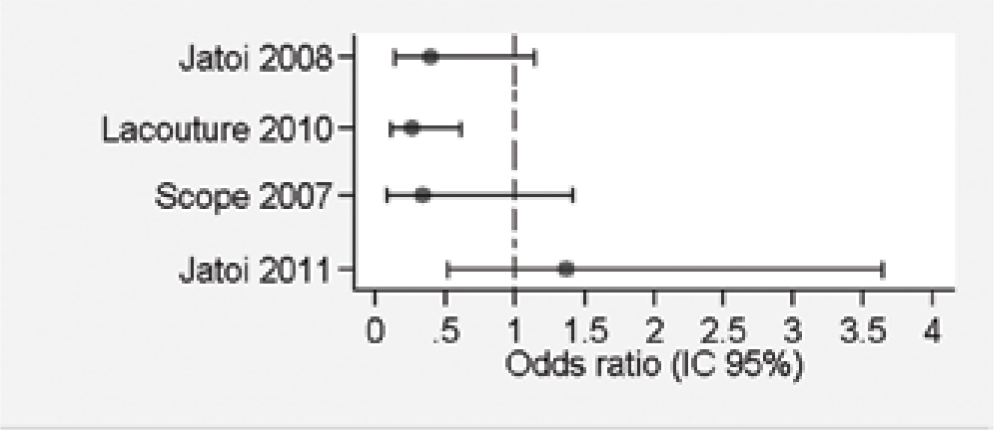
Resultados. Cuatro estudios cumplieron los criterios de selección, comparando la profilaxis con tetraciclinas frente a un placebo y en un estudio frente a manejo reactivo, con el objetivo de disminuir la incidencia de exantema o toxicidades cutáneas de cualquier grado; aunque se encontró una tendencia al efecto protector de las tetraciclinas, solamente en un estudio se observó significancia estadística en cuanto a la disminución de toxicidad cutánea de grado 2.
Conclusiones. A la fecha no es posible tener una recomendación constante sobre la profilaxis con tetraciclinas, si bien hay una tendencia a usar su efecto protector, se requieren más estudios. Palabras clave:inhibidores del receptor de factor de crecimiento epidérmico (EGF), receptor del factor de crecimiento epidérmico (receptor del EGF), tetraciclinas, prevención, exantema pápulo-pustular, ensayos clínicos.
Biografía del autor/a
Claudia Liliana Montoya
Médica, residente de primer año, Servicio de Dermatología, Fundación Valle de Lili-Universidad ICESI, Cali, Colombia
Andrés Vidal
Médico dermatólogo, Fundación Valle del Lili, Cali, Colombia
Magda Cepeda
Médica epidemióloga, Unidad de Investigaciones Clínicas, Fundación Valle del Lili, Cali, Colombia
Referencias bibliográficas
2. Busam KJ, Capodieci P, Motzer R, Kiehn T, Phelan D, Halpern AC. Cutaneous side-effects in cancer patients treated with the antiepidermal growth factor receptor antibody C225. Br J Dermatol. 2001; 144: 1169-76.
3. Lacouture ME. Mechanisms of cutaneous toxicities to EGFR inhibitors. Nature reviews. Cancer. 2006;6:803-12.
4. Joshi SS, Ortiz S, Witherspoon JN, Rademaker A, West DP, Anderson R, et al. Effects of epidermal growth factor receptor inhibitor-induced dermatologic toxicities on quality of life. Cancer. 2010;116:3916-23.
5. Boone SL, Rademaker A, Liu D, Pfeiffer C, Mauro DJ, Lacouture ME. Impact and management of skin toxicity associated with anti-epidermal growth factor receptor therapy: Survey results. Oncology. 2007;72:152-9.
6. Potthoff K, Hofheinz R, Hassel JC, Volkenandt M, Lordick F, Hartmann JT, et al. Interdisciplinary management of EGFR-inhibitorinduced skin reactions: A German expert opinion. Ann Oncol. 2011;22:524-35.
7. Segaert S, van Cutsem E. Clinical signs, pathophysiology and management of skin toxicity during therapy with epidermal growth factor receptor inhibitors. Ann Oncol. 2005;16:1425-33.
8. Robert C, Soria JC, Spatz A, Le Cesne A, Malka D, Pautier P, et al. Cutaneous side-effects of kinase inhibitors and blocking antibodies. Lancet Oncol. 2005;6:491-500.
9. Galimont-Collen AFS, Vos LE, Lavrijsen APM, Ouwerkerk J, Gelderblom H. Classification and management of skin, hair, nail and mucosal side-effects of epidermal growth factor receptor (EGFR) inhibitors. Eur J Cancer. 2007;43:845-51.
10. Pérez-Soler R. Can rash associated with HER1/EGFR inhibition be used as a marker of treatment outcome? Oncology. 2003;17(Suppl.12):23-8.
11. Racca P, Fanchini L, Caliendo V, Ritorto G, Evangelista W, Volpatto R, et al. Efficacy and skin toxicity management with cetuximab in metastatic colorectal cancer: Outcomes from an oncologic/dermatologic cooperation. Clin Colorectal Cancer. 2008;7:48-54.
12. Hu JC, Sadeghi P, Pinter-Brown LC, Yashar S, Chiu MW. Cutaneous side effects of epidermal growth factor receptor inhibitors: Clinical presentation, pathogenesis, and management. J Am Acad Dermatol. 2007;56:317-26.
13. Bachet JB, Peuvrel L, Bachmeyer C, Reguiai Z, Gourraud PA, Bouché O, et al. Folliculitis induced by EGFR inhibitors, preventive and curative efficacy of tetracyclines in the management and incidence rates according to the type of EGFR inhibitor administered: A systematic literature review. Oncologist. 2012;17:555-68.
14. Jatoi A, Dakhil SR, Sloan JA, Kugler JW, Rowland KM, Schaefer PL, et al. Prophylactic tetracycline does not diminish the severity of epidermal growth factor receptor (EGFR) inhibitor-induced rash: Results from the North Central Cancer Treatment Group (Supplementary N03CB). Support Care Cancer. 2011;19:1601-7.
15. Lacouture ME, Anadkat MJ, Bensadoun R-J, Bryce J, Chan A, Epstein JB, et al. Clinical practice guidelines for the prevention and treatment of EGFR inhibitor-associated dermatologic toxicities. Support Care Cancer. 2011;19:1079-95.
16. Fernández-Guarino M, Pérez B, Aldanondo I, García-Millán C, Garrido P, Jaén P. Treatment of acneiform rash by epidermal growth factor inhibitors with oral tetracyclines. Actas Dermosifiliográficas. 2006;97:503-8.
17. Baas JM, Krens LL, Guchelaar H-J, Ouwerkerk J, de Jong FA, Lavrijsen APM, et al. Recommendations on management of EGFR inhibitor-induced skin toxicity: A systematic review. Cancer Treat Rev. 2012;38:505-14.
18. Jatoi A, Rowland K, Sloan JA, Gross HM, Fishkin PA, Kahanic SP, et al. Tetracycline to prevent epidermal growth factor receptor inhibitor-induced skin rashes: Results of a placebo-controlled trial from the North Central Cancer Treatment Group (N03CB). Cancer. 2008;113:847-53.
19. Scope A, Agero ALC, Dusza SW, Myskowski PL, Lieb JA, Saltz L, et al. Randomized double-blind trial of prophylactic oral minocycline and topical tazarotene for cetuximab-associated acne-like eruption. J Clin Oncol. 2007;25:5390-6.
20. Lacouture ME, Mitchell EP, Piperdi B, Pillai MV, Shearer H, Iannotti N, et al. Skin toxicity evaluation protocol with panitumumab (STEPP), a phase II, open-label, randomized trial evaluating the impact of a pre-emptive skin treatment regimen on skin toxicities and quality of life in patients with metastatic colorectal cancer. J Clin Oncol. 2010;28:1351-7.
21. Luu M, Lai SE, Patel J, Guitart J, Lacouture ME. Photosensitive rash due to the epidermal growth factor receptor inhibitor erlotinib. Photodermatol Photoimmunol Photomed. 2007;23:42-5.
22. Duvic M. EGFR inhibitor-associated acneiform folliculitis: Assessment and management. Am J Clin Dermatol. 2008;9:285-94.
Cómo citar
Descargas
Descargas
Publicado
Cómo citar
Número
Sección
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |