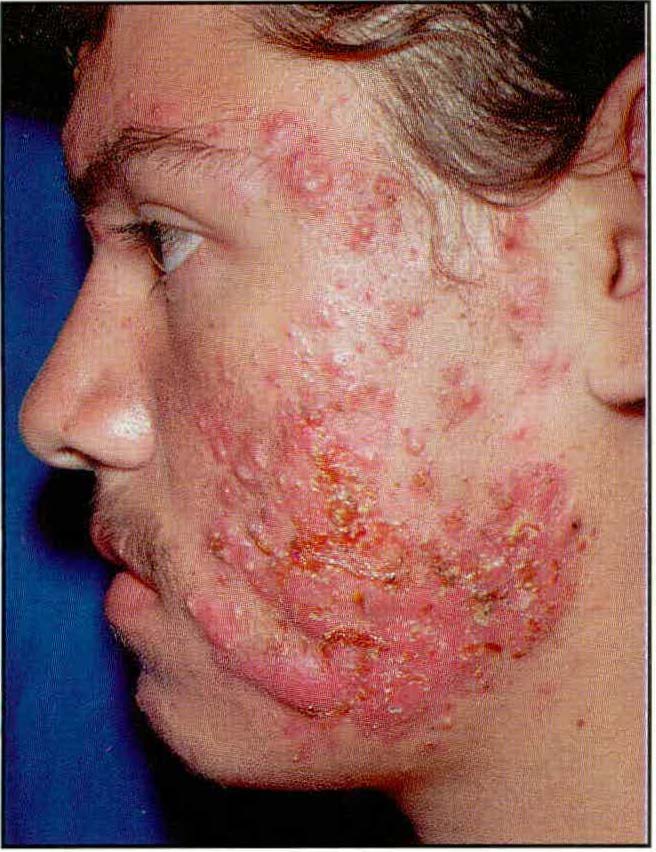
Comparación de la eficacia del trimetoprim-sulfa metoxazol con el clorhidrato de tetraciclina en el tratamiento del acné nódulo-quístico
Palabras clave:
Acné quístico, trimetoprimsulfametoxazol,, tetraciclinaResumen
El tratamiento de elección en el acné nódulo-quístico es la isotretinoína; sin embargo, en nuestro medio muchos pacientes no pueden ser tratados con este medicamento dado su alto costo. El propósito de este estudio fue evaluar la eficacia de la combinación trimetoprimsulfametoxazol, en comparación con el clorhidrato de tetraciclina, en la reducción del número de nódulo-quistes inflamatorios en pacientes con acné quístico. Fueron seleccionados 125 pacientes con diagnóstico clínico de acné quístico, para recibir clorhidrato de tetraciclina (Ambramicinaa), 1 g dos veces al día, por treinta días, y posteriormente 500 mg dos veces al día, por los siguientes dos meses o Trimetoprim Sulfametoxazol , 160/800 mg dos veces al día por treinta días, y posteriormente 80/ 400 mg por los siguientes dos meses. 102 pacientes completaron el estudio y fueron incluídos en el análisis de datos, 51 en cada grupo de tratamiento. Ambos tratamientos fueron igualmente efectivos en la disminución de las lesiones quísticas en este tipo de pacientes (clorhidrato de tetraciclina 88.2%, trimetoprimsulfametoxazol 85.2%, p=0,89), pero se encontró una mayor proporción de efectos colaterales en los pacientes que recibieron clorhidrato de tetraciclina (RR=2, 1 1 ,4<RR<3, 1. Límite de confianza 95%). Ningún paciente presentó efectos colaterales severos como eritema polimorfo mayor. El trimetoprim sulfametoxazol puede ser una alternativa terapéutica eficaz y segura en el tratamiento del acné nódulo-quístico.
Biografía del autor/a
María Cecilia Valbuena Mesa, Centro Dermatológico Federico Lleras Acosta
Dermatóloga, Coordinadora de Pregrado, Docente del Centro Dermatológico «Federico Lleras Acosta», E.S.E.
Luis Arturo Gamboa Suárez, Centro Dermatológico Federico Lleras Acosta
Dermatólogo, Coordinador de Postgrado, Docente del Centro Dermatológico «Federico Lleras Acosta», E.SE
Referencias bibliográficas
2. Strauss J. Sebaccous Glands. En: Fitzpatrick et al. McGraw Hill. 1999, Págs. 769-780.
3. Leyden J. New Understandings ofthe Pathogenesis of Acne. J Am Acad Derrnatol 1995; 32:s15-s25.
https://doi.org/10.1016/0190-9622(95)90416-6
4. Cunliffe W. Tbe Sebaceous Gland and Acne -40 Years On, Derrnatology 1998; 196:9-15.
https://doi.org/10.1159/000017859
5. Meynadier J and Alirezai M. Systernic Antibiotics for Acne. Dermatology 1998; 196:135-139.
https://doi.org/10.1159/000017847
6. Drake L, et al. Guidelines of Care for Acne Vu I garis. J Am Acad Derrnatol 1990; 22 :676-680.
https://doi.org/10.1016/S0190-9622(08)81045-6
7. Prenctiville Jet al. A Comparison ofDapsone with 13-cis retinoic acid in the treatrnent of Nodular Cystic Acne. Clin Exp Dermatol 1988; 13:67-71.
https://doi.org/10.1111/j.1365-2230.1988.tb00659.x
8. Spom M, et al. Mechanism of action of retinoids. J Am Acad Dermatol 1986; 15:756-764.
https://doi.org/10.1016/S0190-9622(86)70231-4
9. Peck G, et al. Isotretion versus Placebo in tbe treatrnent of Cystic Acne. J Am Acad Dermatol 1982; 6:735-745.
https://doi.org/10.1016/S0190-9622(82)70063-5
10. Lester R, et al. Isotretinoin and Tretracycline in the Management of Severe Nodulocystic Acne. IntJ Dermatol 1985; 24:252-257.
https://doi.org/10.1111/j.1365-4362.1985.tb05458.x
11. Bruce S and Wolf J. Antibacterial Agents. En: Wolverton S and Wilkin J. Systernic Drugs for Skin Diseases. W. B. Saunders Company. Philadelphia. 1991; pags. 147-185.
12. Hubbel C, et al. Efficacy ofMinocycline Compared Witb Tetracycline in Treatrnent of Acne Vulgaris. Arch Dermatol 1982; 118:989-992.
https://doi.org/10.1001/archderm.1982.01650240033017
13. Juh]jn L and Liden S, A Quantitative Evaluation of the Effect of oxytetracycline and Doxycycline in Acne VuJgaris. Br J Dermatol 1969; 8l: 154-158.
https://doi.org/10.1111/j.1365-2133.1969.tb15996.x
14. Stern R, et al. Topical vs Systernic Agent Treatrnent for Papulopustular Acne. A Cost-Effectiveness Analysis. Arch Dermatol 1984; 120:1571-1578.
https://doi.org/10.1001/archderm.1984.01650480033013
15. Poulos E and Tedesco F. Acne Vulgaris. Double Blind Tri al Comparing TetracycLine and Clindamycin. Arch Dennatol 1976; 112 :974-976.
https://doi.org/10.1001/archderm.112.7.974
16. Burton N, et al. Neutrophil Chemotaxis in Patietns with Acne Recciving Oral Tetracycline Therapy. Arch Dermato 1 1989; 120: J 308-1313.
17. Esterly N, et al. The Effect of Antimicrobial Agents on Leukocyte Chemotaxis. J lnvest Dennatol 1978; 70-51-55.
https://doi.org/10.1111/1523-1747.ep12543487
18. Halliwell B. et al. Scavenging of Hypochlorous Acid by Tetracycline, Rifampicin and sorne other Antibiotics; A Possible Antioxidant Action ofRifampicin and TetracycLine?. Bioch Pharm 1988:37.775-778
https://doi.org/10.1016/0006-2952(88)90159-1
19. lngham E. et al. Pro-lnflamatory Levels of lnterleukin-la-Like Bioactivity are Present in the Majority ofOpen Comedones In Acne Vulgaris. J lnvest Dermatol 1992; 98:895-90 l.
https://doi.org/10.1111/1523-1747.ep12460324
20. Eady E, et al. Modulation of Comedonal Levels of lnterleukin-1 in Acne Patients Treated with Tetracycl ines. J Invest Dermatol 1993; 101:86-91.
https://doi.org/10.1111/1523-1747.ep12360123
21. Baer R, et al. High-Dose Tetracycline therapy in Severe Acne. Arch Dermatol 1976; 112:479-481.
https://doi.org/10.1001/archderm.1976.01630280009002
22. Cotteril J, et al. A Comparison ofTrimethoprimSulphamethoxazole with Oxytetracycline in Acne Vulgaris. Br J Dermatol 1971; 84:366-369.
https://doi.org/10.1111/j.1365-2133.1971.tb14233.x
23. Gibson J, et al. oral Trimethoprim versus Oxytetracycline in the Tretament of lnflamatory Acne Vulgaris. Br J Dermatol 1982,107:221-224.
https://doi.org/10.1111/j.1365-2133.1982.tb00342.x
24. Strauss J and Pochi P. The Effect of Sulfisoxazole-Trimethoprim Combination on Ti tratable Acidity of Human Sebum. Br J Dermatol 1970; 82:493-496.
https://doi.org/10.1111/j.1365-2133.1970.tb02210.x
25. Coleman M. Dapsone. Modes of Action, Toxicity and Possible Strategies for lncreasing Patient Tolerance 1993; 129:507-513.
https://doi.org/10.1111/j.1365-2133.1993.tb00476.x
26. Lang P. Sulfones and Sulfonarnides in Dermatology Today. J Am Acad Dermatol 1979, 1:479-492.
https://doi.org/10.1016/S0190-9622(79)80088-2
27. Barranco V. Dapsone-Other indications. lnt J Dermatol. 1982. 21: 513-515.
https://doi.org/10.1111/j.1365-4362.1982.tb01195.x
28. Karninsky C, et al. Acne: Treatrnent with Diaminodiphenysu 1 fone. Cutis 1984; 13:869-872.
https://doi.org/10.1038/sj/leu/2401430
29. Thuong-Nguyen V, et al. Inhibition of Neutrophil Adherence to antibody by Dapsone: A Possible Terapeutic Mechanism of Dapsone in thc Treatment of lgA Dermatoses. J Invest Dennatol 1993, 100:34 9-355.
https://doi.org/10.1111/1523-1747.ep12471811
30. Ban-anco V. [nhibition ofLysosomal Enzymes by Dapsone. Arch Dennatol 1974; 110:563-566.
https://doi.org/10.1001/archderm.110.4.563
31. Cotteril J, et al. The Effect ofThrimethoprim-Sulphan1ethoxazole on Sebum Excretion rate and Biochernistry in Acne Vulgaris. Br J Dermatol 1971; 85: l 30-133.
https://doi.org/10.1111/j.1365-2133.1971.tb07197.x
32. Strom B, et al. A PopuJation Based Study of Stevens-Johnson Syndrome. Arch Dermatol 1991: 127:831-838.
https://doi.org/10.1001/archderm.127.6.831
Cómo citar
Descargas
Descargas
Publicado
Cómo citar
Número
Sección
| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |